■ 产品描述
人CD8+T细胞分选试剂盒是通过阴性分选法从人外周血单个核细胞(PBMC)中分离出 CD8+T细胞。原理是利用生物素(biotin)标记的单克隆抗体对非目标细胞(非CD8+T细胞)进行标记,然后通过链霉亲和素(streptavidin)标记的磁珠对非目标细胞进行清除,从而达到纯化人CD8+T细胞的目的。分选过程需要用到磁力架。
■ 产品组分

■ 储存条件
2-8°C保存,不可冷冻,有效期见试管标签。
■ 适用范围
本试剂盒适用于从新鲜分离的人 PBMC 或冻存的人 PBMC 中分选出CD8+T细胞。
■ 操作流程
1.制备人PBMC:利用 Ficoll 密度梯度离心法从人外周血中分离 PBMC,收集 PBMC,以 PBS 洗涤细胞,离心后将 PBMC 重悬于分选 buffer 中,调整细胞密度为 1×10^8 cells/mL。
注意:分选buffer为含有2% FBS和2mM EDTA的PBS ,缓冲液应该不含Ca2+和Mg2+ ,需预先通过0.22 μm滤膜过滤除菌。
2. 抗体标记非目的细胞:将 100 μL 细胞悬液( 1×10^7个细胞)加入一个无菌 1.5 mL 离心管底部,再加入 2 μL Biotin-Antibody Mix,混匀后 4°C 孵育 15 min。加入1 mL(10倍体积)分选buffer,500 g离心5分钟,弃上清,用100 μL缓冲液重悬细胞。
注意:按比例调整用量:如5×10⁷ cells需500 μL细胞悬液 + 10 μL抗体,用5 mL分选buffer洗涤。可以使用 15 mL 或 50 mL 离心管进行操作。
3. 磁珠预处理:涡旋震荡重悬磁珠(Streptavidin-beads),吸取20 μL磁珠至1.5 mL离心管,加入1 mL分选buffer,10000 g离心1 min,弃上清。重复洗涤1次。清洗后用20 μL分选buffer进行重悬。
注意:buffer与磁珠最终是1:1等比例混匀,如清洗50 μL磁珠(Streptavidin-beads),则最终用50 μL buffer重悬。
4. 磁珠孵育:加入10 μL预处理过的Streptavidin-beads混悬液,轻轻混匀,4℃孵育10分钟。
注意:说明书以1×10^7个细胞量举例,如果分选更多细胞,则按比例增加Streptavidin-beads用量。
5. 磁力分离:孵育完成后,将细胞和磁珠混合液转移至一个无菌5 mL流式管中,补加分选 buffer 至总体积为 2.5 mL,用移液器吹打5次混匀。将流式管置于磁力架上静置5分钟。
注意:流式管选用聚苯乙烯材质。
6. 收集细胞 :手持磁力架,将细胞悬液轻柔倒入无菌离心管中,此细胞悬液中即包含纯化的人CD8+T细胞。
注意:倾倒过程中流式管不要脱离磁力架。
7.二次纯化(可选*):将收集的细胞悬液离心,500 g离心5 min后,弃上清,用 100 μL 分选 buffer 重悬细胞,重复步骤4-6,此操作可提高纯度2-4%。
■ 注意事项
1.磁珠和抗体混合液使用和保存过程中均应避免冷冻、高速离心等操作;
2.建议选用低吸附移液器吸头和离心管,避免因吸附造成磁珠和抗体的损耗;
3.如果单次分选少于1×10^7 cells,则将细胞悬液体积补至100 μL ,加入2 μL Biotin-Antibody Mix和10 μL Streptavidin-Beads;
4.本产品需与磁性分离器配套使用;
5.本产品仅供研究使用。
■ 分选效果
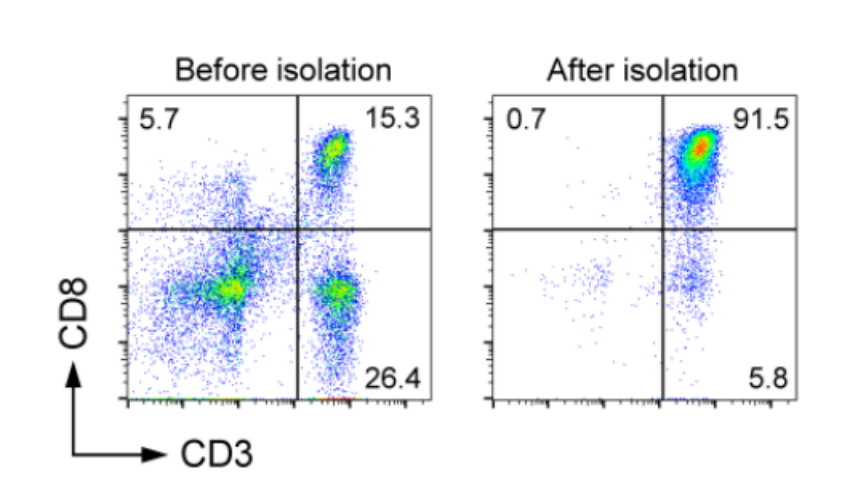
从人 PBMC 中分选CD8+T 细胞,用 PE 标记的 anti-human CD8a 抗体(克隆号 RPA-T8)和 APC 标记的 anti-human CD3 抗体(克隆号 OKT3)染色后进行流式细胞分析,分选前后的 CD3+CD8+T细胞纯度分别为 15.3%和 91.5%。