■ 产品描述
小鼠中性粒细胞分选试剂盒是通过阴性分选法从小鼠骨髓或其它组织样本的单细胞悬液中分离出中性粒细胞。原理是选用生物素(bioti-n)标记的单克隆抗体对非目标细胞(非CD11b+Ly-6G+细胞)进行标记,而后通过链霉亲和素(streptavidin)标记的磁珠去除非目标细胞,从而达到小鼠中性粒细胞分选的目的。分选过程需要用到磁力架。
■ 产品组分

■ 储存条件
2-8°C保存,不可冷冻,有效期见试管标签。
■ 适用范围
本试剂盒适用于分选小鼠骨髓、外周血或脾脏中性粒细胞。
■ 细胞样品制备
1.获取小鼠骨髓、脾脏或外周血细胞于离心管中,进行红细胞裂解。
注意:红细胞裂解步骤可根据组织样本及所用裂解液的不同调整用量及时间,通常小鼠外周血红细胞裂解需要的时间更长。少量红细胞残留不会影响分选细胞纯度,骨髓细胞不裂解红细胞也可直接进行分选,但分选细胞纯度可能随红细胞占比增加有5%以内小幅度下降。
2.裂解完成后,PBS重悬细胞,将细胞悬液用70 μm细胞筛网过滤,500 g,离心5 min。
注意:细胞悬液需要过细胞筛网,以除去组织和细胞团块,否则会影响后续细胞分选纯度。
3.离心完成后,将细胞重悬于分选Buffer,洗涤细胞,500 g离心5 min,弃上清。
注意:分选buffer为含有2mM EDTA和2%胎牛血清(FBS)的PBS或者含有2mM EDTA和0.5%BSA的PBS,需预先通过0.22 μm滤膜过滤除菌。缓冲液应该不含Ca2+和Mg2+。
4.将细胞重悬于分选buffer中,调整细胞密度为1×10^8 cells/mL。
■ 分选流程
1.将100 μL细胞悬液(1×10^7个细胞)加入1.5 mL离心管底部,再加入2 μL Biotin-Antibody Mix,混匀后4℃孵育10 min。
注意:加入细胞悬液时将细胞加入离心管底部,避免沿管壁加入。如果分选更多细胞,则按比例增加Biotin-Antibody Mix的用量。
2.孵育完成后,洗涤细胞1次:补分选Buffer至1.5 mL,500 g离心5 min。
注意:若分选的细胞数目过多,则使用15 mL离心管,补分选Buffer至5-10 mL后离心。
3.离心完成后,弃上清,用100 μL分选Buffer重悬细胞。
注意:如果分选更多细胞,则按比例增加分选buffer用量。
4.磁珠使用前需要用分选buffer进行清洗:涡旋震荡重悬磁珠(Streptavidin-beads),吸取20 μL磁珠至1.5 mL离心管,加入1 mL分选buffer,10000 g离心1 min,弃上清。重复洗涤磁珠1次。清洗后用20 μL分选buffer进行重悬。
5.在离心管中加入20 μL清洗过的Streptavidin-Beads混悬液,充分混匀后4℃孵育10 min。
注意:如果分选更多细胞,则按比例增加Streptavidin-Beads用量。
6.孵育完成后,转移至流式管中,补分选buffer至2.5mL,用移液器上下混合充分混匀(避免剧烈振荡或者上下颠倒混匀)。
7.将含有细胞的分选流式管置于磁力架上,静置5 min。
8.将细胞悬液轻柔倒入一个无菌离心管中(倾倒过程中流式管不要脱离磁力架),此细胞悬液中即包含纯化的小鼠中性粒细胞,500 g,离心5 min。离心后弃上清,收集细胞。
9.根据实验需要洗涤细胞后,将细胞重悬于所需缓冲液或培养基中,即可用于后续分子生物学或细胞生物学实验。
■ 注意事项
1.磁珠和抗体混合液使用和保存过程中均应避免冷冻、高速离心等操作;
2.建议选用低吸附移液器吸头和离心管,避免因吸附造成磁珠和抗体的损耗;
3.如果单次分选少于1×10^7 cells,则将细胞悬液体积补至100 μL,加入2 μL Biotin-Antibody Mix和20 μL Streptavidin-Beads;
4.说明书以1×10^7个细胞量举例,如果分选更多细胞,则按比例增加试剂用量。例如分选5×10^7 cells,则在500 μL细胞悬液中加入10 μL Biotin-Antibody Mix和100 μL Streptavidin-Beads;
5.本产品需与磁性分离器配套使用;
6.本产品仅供研究使用。
■ 分选效果
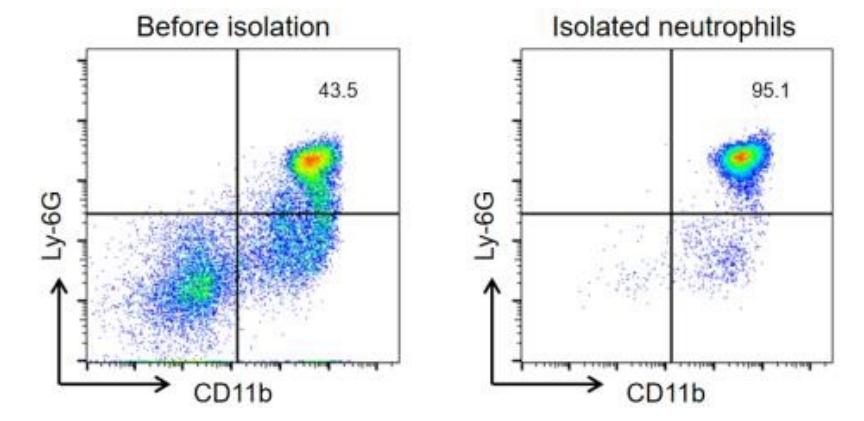
从C57BL/6小鼠骨髓细胞中分选中性粒细胞,分选前后的细胞用FITC anti-mouse Ly-6G抗体(克隆号1A8)和PE anti-mouse CD11b抗体(克隆号M1/70)标记后进行流式细胞仪分析,分选前后的中性粒细胞纯度分别为43.5%和95.1%。