■ 产品描述:
人单核细胞分选试剂盒通过免疫磁珠阴选,在短至15分钟内从新鲜或冻存的人外周血单核细胞(PBMCs)或洗涤的白细胞单采术样本中分离出高度纯化的CD14+CD16-单核细胞。该试剂盒通过靶向非单核细胞表面标志物的抗体去除非单核细胞,非目的细胞用抗体和磁珠标记,并使用磁极进行无柱分选。目的细胞被简单地倾倒入新管中即可。分选后的细胞可立即用于下游应用,如流式细胞术、培养或DNA/RNA提取。
■ 产品信息:

■ 储存条件:2-8°C保存,不可冷冻,有效期见试管标签。
■ 设备和试剂要求:
分选缓冲液:PBS,pH 7.2,0.5%BSA,2 mM EDTA
Ficoll细胞分离液、无菌红细胞裂解液、计数液
耗材:离心管、无菌流式管
仪器:离心机、磁力架
■ 样本制备:
1.外周血样本
EDTA的存在对本试剂盒的性能非常重要。使用K2EDTA或K3EDTA作为抗凝剂采集血液。如果使用非EDTA的抗凝剂,则必须在全血样本中加入最终浓度为3 mM的EDTA。
通过使用密度梯度离心液离心,从全血中制备外周血单个核细胞(PBMC)悬液。如果使用冻存的PBMC,在室温(15-25°C)下用终浓度100 μg/mL的DNase I溶液孵育细胞至少15分钟,再进行标记和分选。使用37 μm的细胞过滤器过滤细胞悬液去除聚团,以获得最佳结果。制备完成后,将细胞以5×10^7细胞/mL的浓度重悬于推荐的缓冲液中。
2.白细胞单采术样本
加入等体积的分选缓冲液,在室温(15-25°C)下以120 g离心10分钟,清洗外周血白细胞单采样本,重复清洗一遍。如果需要裂解红细胞(RBC),请在第一次清洗步骤前使用氯化铵溶液进行裂解。去除上清液,并将细胞以5×10^7细胞/mL的浓度重悬于分选缓冲液中。
■ 注意事项:
1.本产品仅适用于体外细胞培养,不可直接用于临床治疗。
2.去除血小板:人血小板去除试剂在用于按照样本制备流程从人外周全血制备的新鲜PBMC时,效果最佳。人血小板去除试剂用于白细胞单采术样本或冻存的PBMC样本时,可能会导致单核细胞回收率降低。
■ 操作流程:
1.取1×10^7细胞加入到5 mL流式管中。
2.加入10 μL抗体混合物。
3.(可选)加入10 μL血小板去除试剂。
4.混匀后室温孵育5 min。
5.加入10 μL磁珠,混匀后室温孵育5 min,磁珠使用前应充分混匀。
6.加入2 mL分选缓冲液,使用移液器吹打混匀,置于磁极中,室温静置5 min。
7.拿起磁力架,以一个连续的动作将磁力架和试管倒置,将富集的细胞悬液倒入新试管中。倒出的细胞即为目的细胞。
注:▲以上步骤给出的试剂推荐用量可处理1×10^7个总细胞,若细胞数量少于1×10^7,则按1×10^7个细胞加入试剂;若细胞数量多于1×10^7,应按比例相应增加试剂用量。
▲尽量快速操作,保持细胞冷却,并使用预冷溶液,以减少非特异性细胞标记。
▲磁珠与细胞孵育时需要温和地彻底混匀,以提高分选效率。
■ 分选效果:
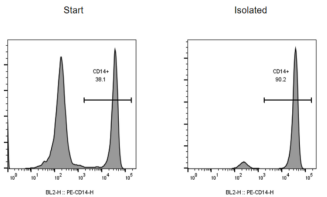
使用人单核细胞分选试剂盒从PBMC中分离单核细胞。用CD14-PE对分离出的细胞进行荧光染色,并通过流式细胞术进行分析,分选前后的CD14+细胞纯度分别为38.1%和90.2%。